O que são os leucócitos?
Existem três tipos de células circulando pelo nosso sangue:
- Hemácias: também chamadas de glóbulos vermelhos. São as células responsáveis pelo transporte de oxigênio e gás carbônico pelo sangue.
- Leucócitos: também conhecidos como glóbulos brancos. Fazem parte do sistema imunológico.
- Plaquetas: não são propriamente células, mas sim fragmentos de um grupo de células chamadas megacariócitos.
Os leucócitos, tema deste artigo, desempenham um papel essencial na defesa do corpo humano contra agentes patogênicos, como bactérias, vírus, fungos ou parasitos.
Nota: este artigo é longo e aborda diversos pontos sobre os leucócitos, que é um assunto complexo. Para facilitar a compreensão, algumas informações e conceitos serão simplificados e propositalmente repetidos ao longo das seções do texto para ajudar na aprendizagem do conteúdo.
Como são produzidos os leucócitos?
Os leucócitos são produzidos pela medula óssea, um tecido esponjoso encontrado no interior de ossos como o fêmur, as costelas, a pelve e o esterno.
A produção dos leucócitos tem início em um tipo especial de célula chamada célula-tronco hematopoiética. As células-tronco hematopoiéticas são células indiferenciadas, o que significa que elas têm a capacidade de se transformar em diferentes tipos de células do sangue, incluindo qualquer uma das três linhagens de células sanguíneas: leucócitos, hemácias e megacariócitos.
Durante o processo de diferenciação, as células-tronco hematopoiéticas passam por várias etapas, dando origem a tipos específicos de leucócitos, que, ao amadurecerem, são liberados na corrente sanguínea. Esse processo é altamente regulado, sendo ajustado conforme as necessidades do organismo. Por exemplo, durante uma infecção, a medula óssea aumenta a produção de leucócitos para ajudar a combater o agente invasor (explicaremos melhor esse mecanismo mais adiante).
Os leucócitos podem ser divididos em dois grandes grupos, a partir das suas células progenitoras na medula óssea: os leucócitos derivados da célula-tronco mieloide e os leucócitos derivados da célula-tronco linfoide. Essa classificação reflete a linhagem celular de onde eles se originam, influenciando suas funções no sistema imunológico.
1. Leucócitos derivados da célula-tronco mieloide
Esses leucócitos são parte principalmente da resposta imune inata e incluem:
- Neutrófilos.
- Eosinófilos.
- Basófilos.
- Monócitos.
- Células dendríticas.
- Macrófagos.
2. Leucócitos derivados da célula-tronco linfoide
Esses leucócitos fazem parte principalmente da resposta imune adaptativa e incluem:
- Linfócitos T.
- Linfócitos B.
- Plasmócitos.
- Células NK (Natural Killers).
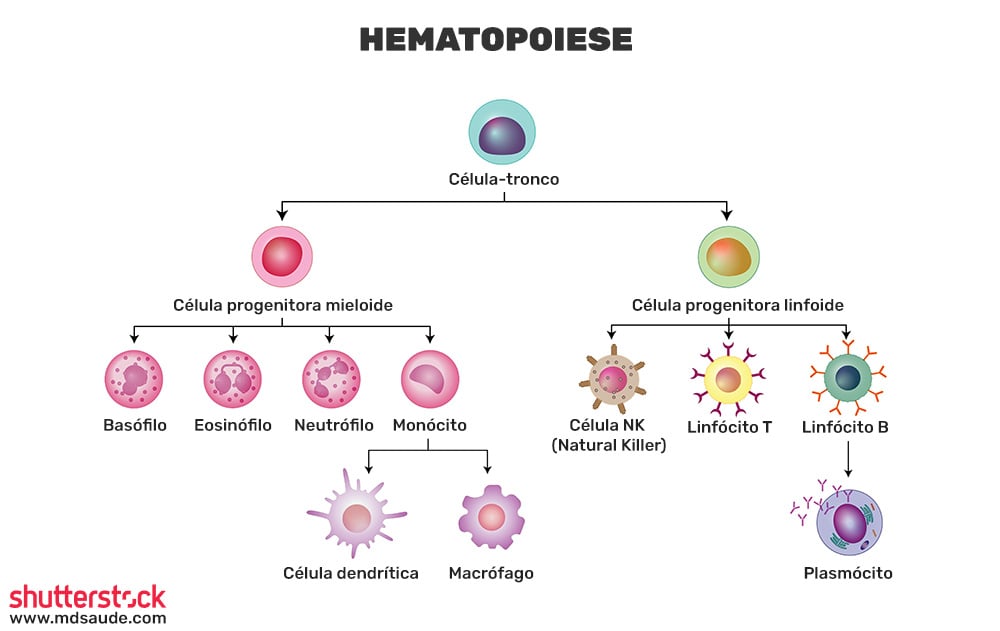
Outra forma possível de dividir os leucócitos é baseada na presença ou ausência de grânulos em seu citoplasma, que são visíveis ao microscópio.
Nessa forma de classificação, dois grupos se formam: os granulócitos e os agranulócitos:
- Granulócitos:
- Neutrófilos.
- Eosinófilos.
- Basófilos.
- Agranulócitos:
- Linfócitos.
- Monócitos.
Explicaremos os diferentes tipos de leucócitos a partir dessa forma de divisão.
Leucócitos granulócitos
Os leucócitos granulócitos, também chamados de granulócitos, são um tipo específico de leucócito que possuem grânulos em seu citoplasma, daí o nome “granulócitos”. Esses grânulos são estruturas intracelulares que contêm diversas enzimas e substâncias químicas, cuja função é auxiliar no combate a agentes infecciosos e na resposta inflamatória.
Os granulócitos são parte importante da imunidade inata, que é a primeira linha de defesa contra infecções e não depende do reconhecimento específico dos patógenos. São células de defesa “generalistas”, atacam qualquer tipo de invasor que identifiquem.
Os granulócitos são classificados em três tipos principais: neutrófilos, eosinófilos e basófilos. Cada tipo possui características específicas que os tornam mais eficazes em determinados contextos de defesa.
Neutrófilos
Os neutrófilos são os leucócitos mais abundantes no sangue, representando cerca de 50% a 70% do total de glóbulos brancos. Eles são os primeiros a responder a infecções bacterianas e fúngicas. Os neutrófilos são especializados em fagocitar, ou seja, engolfar e digerir microrganismos invasores. Eles também liberam substâncias que auxiliam na destruição dos patógenos. A sua rápida resposta é um aspecto essencial do sistema imunológico inato.
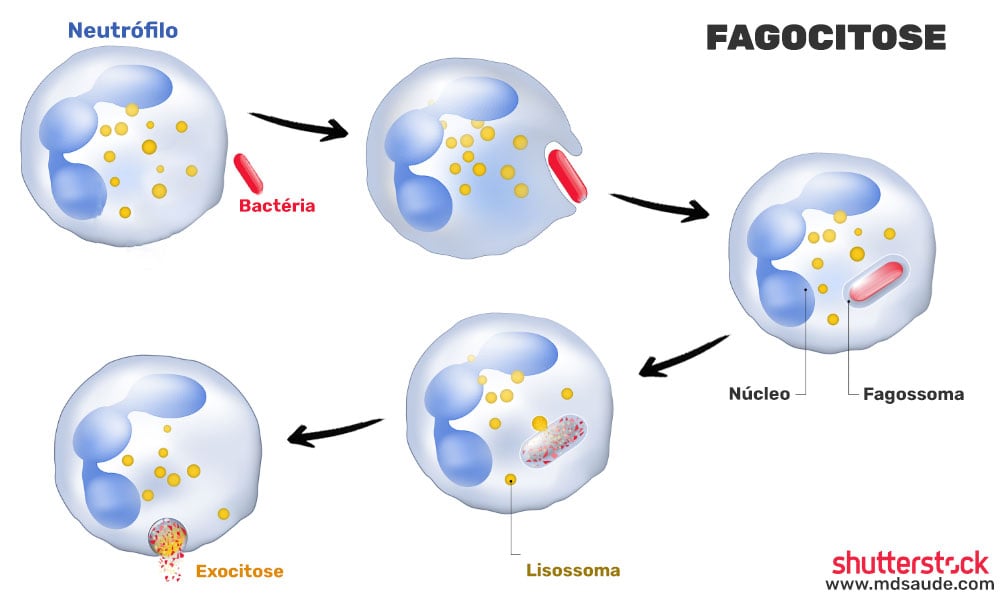
Os neutrófilos têm uma vida curta, geralmente em torno de 6 a 12 horas na circulação sanguínea, e morrem rapidamente após realizarem suas funções, formando parte do pus encontrado em infecções.
Eosinófilos
Os eosinófilos são menos abundantes que os neutrófilos, representando cerca de 1% a 4% do total de leucócitos. Eles são particularmente importantes na resposta imunológica contra parasitos, como helmintos (vermes), e também desempenham um papel relevante no surgimento das reações alérgicas.
Os eosinófilos são especialmente eficazes na defesa contra parasitas multicelulares, como vermes. Como esses parasitas são muito grandes para serem fagocitados, os eosinófilos aderem à superfície dos parasitas e liberam o conteúdo de seus grânulos, que contêm enzimas citotóxicas capazes de danificar a membrana do parasita e levar à sua morte.
Os eosinófilos também liberam mediadores inflamatórios, como leucotrienos, e enzimas como a peroxidase eosinofílica, que ajudam a intensificar a resposta inflamatória. Níveis elevados de eosinófilos são frequentemente encontrados em pessoas com alergias, como asma, urticária ou rinite alérgica.
Basófilos
Os basófilos são os granulócitos menos comuns, representando menos de 1% dos leucócitos no sangue. Eles têm um papel importante em reações de hipersensibilidade imediata (como em alergias) e na resposta inflamatória. Os basófilos compartilham algumas características com os mastócitos, que são outro tipo de células de defesa encontradas nos tecidos (como os mastócitos não são um tipo de leucócito, eles não serão abordados neste artigo).
Os basófilos estão envolvidos nas reações alérgicas e na resposta inflamatória, liberando histamina e outras substâncias que promovem a dilatação dos vasos sanguíneos e aumentam a permeabilidade dos capilares, facilitando o recrutamento de outros leucócitos para o local da inflamação.
Leucócitos agranulócitos
Os leucócitos agranulócitos, ou simplesmente agranulócitos, são um grupo de leucócitos que se distinguem dos granulócitos pela ausência de grânulos visíveis no citoplasma quando observados ao microscópio.
Embora não possuam esses grânulos típicos, são igualmente essenciais para a defesa do organismo, desempenhando papéis fundamentais tanto na imunidade inata quanto na imunidade adaptativa.
Enquanto os granulócitos são células de defesa “generalistas”, os agranulócitos podem ser considerados células de defesa mais “especializadas”, pois são produzidas com intuito de atacar especificamente um determinado tipo de invasor.
Os agranulócitos são classificados em dois tipos principais: linfócitos e monócitos.
Linfócitos
Os linfócitos são um dos principais tipos de leucócitos agranulócitos, e eles desempenham um papel crucial na imunidade adaptativa, que é a resposta mais específica e sofisticada do sistema imune.
Os linfócitos representam cerca de 20% a 40% dos leucócitos no sangue periférico e são encontrados em grandes quantidades nos tecidos linfoides, como linfonodos, baço, amígdalas e timo.
Os linfócitos podem ser divididos em três tipos principais:
1. Linfócitos B
Os linfócitos B são responsáveis pela produção de anticorpos. Quando ativados por um antígeno específico, os linfócitos B se transformam em plasmócitos, células especializadas na produção e liberação de grandes quantidades de anticorpos. Esses anticorpos se ligam ao patógeno específico, neutralizando-o ou marcando-o para destruição por outras células do sistema imunológico.
Os linfócitos B também são importantes para a memória imunológica. Após uma infecção, alguns linfócitos B se transformam em células de memória, que permanecem no organismo por longos períodos e garantem uma resposta rápida e eficaz caso o mesmo patógeno volte a invadir o corpo.
2. Linfócitos T
Os linfócitos T têm diversas funções na regulação e execução da resposta imune, sendo divididos em várias subcategorias:
- Linfócitos T Auxiliares (CD4+): também chamados de células T helper, esses linfócitos têm um papel crucial na coordenação da resposta imunológica. Eles liberam citocinas, que são moléculas sinalizadoras que ajudam a ativar outras células imunes, como linfócitos B, macrófagos e células T citotóxicas.
- Linfócitos T Citotóxicos (CD8+): também conhecidos como células T killer, esses linfócitos reconhecem e destroem células infectadas por vírus ou células tumorais. Eles têm a capacidade de induzir a morte celular programada (apoptose) nas células-alvo, garantindo que o patógeno intracelular seja eliminado junto com a célula infectada.
- Linfócitos T Supressores/Reguladores: esses linfócitos ajudam a regular e “desligar” a resposta imune após a eliminação do patógeno, evitando uma resposta excessiva que poderia causar danos aos tecidos saudáveis do corpo. Eles são essenciais para prevenir doenças autoimunes, nas quais o sistema imunológico ataca erroneamente as células do próprio organismo.
3. Linfócitos NK (Natural Killers)
Os linfócitos NK (natural killers) são uma subcategoria de linfócitos que fazem parte da imunidade inata. Eles têm a capacidade de reconhecer e destruir células infectadas por vírus ou células tumorais sem a necessidade de um reconhecimento prévio de antígenos. Eles são chamados de “assassinos naturais” porque atuam de forma rápida e não específica, diferentemente dos linfócitos B e T, que requerem ativação específica por antígenos.
Monócitos
Os monócitos são outro tipo importante de agranulócito, representando cerca de 2% a 8% dos leucócitos circulantes.
Os monócitos são leucócitos pertencentes à imunidade inata e circulam no sangue até serem recrutados para locais de infecção ou inflamação. Uma de suas principais características é a capacidade de migrar para os tecidos, onde se diferenciam em outros tipos de células, como macrófagos ou células dendríticas, dependendo das necessidades do organismo e do microambiente no local.
Quando se diferenciam em macrófagos, os monócitos atuam como células imunes residentes nos tecidos, desempenhando papel tanto na defesa do organismo quanto na remoção de células mortas e na regulação da inflamação. Os macrófagos liberam citocinas que modulam a resposta imune, recrutando outras células para o local da inflamação e ajudando a iniciar o reparo tecidual.
Outra importante função dos macrófagos é a fagocitose, ou seja, a capacidade de engolfar e digerir patógenos, células mortas e detritos celulares, sendo extremamente eficazes na limpeza de áreas de infecção ou inflamação.
Já os monócitos que se diferenciam em células dendríticas são fundamentais para a apresentação de antígenos. As células dendríticas capturam antígenos de patógenos, processam esses antígenos e os apresentam na superfície para os linfócitos T. Esse processo é essencial para iniciar a resposta imune adaptativa, uma vez que os linfócitos T só podem ser ativados se reconhecerem os antígenos apresentados pelas células dendríticas (veja exemplos mais adiante).
Temos macrófagos e células dendríticas espalhados por vários tecidos do corpo, servindo como “seguranças”. São geralmente as primeiras células de defesa a serem ativadas quando um patógeno invade nosso corpo. Há macrófagos e células dendríticas nas vias respiratórias altas e baixas, nas mucosas, nas camadas inferiores da pele, no figado (onde são chamados de células de Kupffer), no cérebro, nos intestinos, etc.
Resumindo o que foi explicado até agora:
A imunidade inata é a primeira linha de defesa do organismo, composta por barreiras físicas (como pele e mucosas) e células fagocíticas (como neutrófilos e macrófagos) que respondem rapidamente e de forma inespecífica a qualquer agente invasor. É imediata, mas não possui memória imunológica, ou seja, responde da mesma forma a infecções repetidas.
A imunidade adaptativa, por outro lado, é mais lenta, mas altamente específica. Ela envolve linfócitos T e B, que reconhecem e atacam patógenos específicos e formam células de memória. Isso permite uma resposta mais rápida e eficaz em futuras exposições ao mesmo agente infeccioso.
Como os leucócitos agem contra invasores?
Ainda reforçando o que já foi explicado: os leucócitos têm várias funções que são essenciais para a manutenção das defesas do corpo. Eles atuam principalmente na detecção, reconhecimento, ataque e eliminação de microrganismos patogênicos e células anormais. Essas funções são realizadas por meio de vários mecanismos, incluindo:
- Fagocitose: algumas células, como os neutrófilos e os monócitos/macrófagos, englobam e digerem partículas estranhas ou microrganismos. Esse processo é fundamental para a eliminação direta de invasores.
- Produção de anticorpos: os linfócitos B produzem anticorpos específicos para cada antígeno, que são moléculas encontradas na superfície dos patógenos. Esses anticorpos se ligam aos antígenos, neutralizando-os ou marcando-os para serem destruídos por outras células do sistema imunológico.
- Liberação de mediadores químicos: leucócitos como basófilos e eosinófilos liberam substâncias químicas, como histamina, que são importantes na modulação da inflamação e na resposta alérgica. A inflamação é um processo que visa isolar e eliminar o agente nocivo, além de iniciar o reparo tecidual.
- Resposta citotóxica: os linfócitos T citotóxicos e os linfócitos NK são responsáveis pela destruição direta de células que estão infectadas por vírus ou que são cancerígenas, ajudando a evitar a proliferação de células danificadas ou malignas.
Exemplos de ação dos leucócitos contra germes invasores
Citamos a seguir quatro exemplos de como os leucócitos interagem entre si para controlar uma infecção ou o surgimento de cânceres. Esses processos estão explicados separadamente apenas para facilitar o entendimento. Em geral, eles ocorrem em simultâneo e mais de uma linhagem de leucócitos é recrutada para o combate.
Exemplo 1: ação dos neutrófilos na fagocitose de bactérias
Imagine que você teve uma ferida na pele e, a partir dessa porta de entrada, bactérias conseguiram penetrar no seu corpo. A presença dessas bactérias invasoras é reconhecida por células imunológicas residentes na epiderme, como os macrófagos e as células dendríticas.
Ao notar a invasão, os macrófagos e outras células liberam citocinas e quimiocinas, que são sinais de alerta que atraem neutrófilos para o local da infecção. Além disso, as células da região também liberam substâncias que promovem a vasodilatação, permitindo um aumento no fluxo sanguíneo e facilitando a chegada dos leucócitos. Essa vasodilatação é a responsável pela pele ficar quente e avermelhada nas infecções.
Os neutrófilos que circulam na corrente sanguínea reconhecem esses sinais químicos e vão em direção ao local onde eles estão sendo produzidos. Esse processo chama-se quimiotaxia, ou seja, os neutrófilos do sangue movem-se em direção ao gradiente de concentração de quimiocinas que indica o local da infecção.
Enquanto o reforço dos neutrófilos não chega, os macrófagos começam o processo de combate por meio de fagocitose.
Ao chegar perto dos vasos sanguíneos na área afetada, os neutrófilos aderem à parede do vaso sanguíneo e o atravessam, em um processo chamado diapedese, migrando para o tecido infectado.
No local da infecção, os neutrófilos identificam as bactérias por meio de receptores em sua superfície. Eles então realizam a fagocitose, envolvendo e destruindo a bactéria rapidamente, evitando que a infecção se espalhe. O pus que muitas vezes surgem nas infecções é uma mistura de restos de bactérias, células e neutrófilos mortos, enzimas produzidas durante o processo e fluidos que extravasam dos vasos sanguíneos como parte do processo inflamatório.
Exemplo 2: ativação dos linfócitos T citotóxicos contra células infectadas por vírus
Os vírus causam infecção ao invadir nossas células e “raptar” a maquinaria interior para produzir novos vírus. Ou seja, as células infectadas deixam de desempenhar suas funções e se transformam em fábricas de produzir cópias do vírus invasor.
Quando a célula é capturada por um vírus, ela ainda consegue emitir um sinal de alerta para o sistema imunológico. Ela pega uma proteína desse vírus e a deixa exposta em sua superfície, como se fosse uma placa dizendo “estou infectada”.
Essas células infectadas são reconhecidas pelas células dendríticas. As células dendríticas capturam essa proteína viral, viajam até os linfonodos e onde encontram os linfócitos T citotóxicos virgens, que ainda não estão preparados para atacar diretamente nenhum invasor. As células dendríticas “apresentam” as proteínas do vírus aos linfócitos T, como se estivesse mostrando uma foto do invasor e dizendo: esse é o alvo que você precisa atacar.
Ao ser apresentado ao invasor, os linfócitos T se ativam, tornando-se linfócitos T citotóxicos efetores (CD8+), e vão atrás das células invadidas pelo vírus ao qual eles foram apresentados.
Ao encontrar as células infectadas, o linfócito T citotóxico se liga a ela e libera substâncias que criam poros na membrana da célula comprometida. Isso facilita a entrada de enzimas proteolíticas que desencadeiam o processo de fragmentação do material genético do vírus e da célula, provocando a destruição de ambos.
Exemplo 3: ativação dos linfócitos B produzindo anticorpos contra bactérias
Neste exemplo, usaremos o Streptococcus pneumoniae, que é uma bactéria que habitualmente causa pneumonia.
Quando uma bactéria invasora entra nas nossas vias aéreas, ela é reconhecida por células do sistema imune inato, como macrófagos e células dendríticas que vivem nessa região. As células dendríticas fagocitam a bactéria e apresentam fragmentos desta em sua superfície. Elas então migram para os linfonodos, onde irão se encontrar com linfócitos T.
Nos linfonodos, as células dendríticas apresentam o antígeno bacteriano aos linfócitos T auxiliares (CD4+), que reconhecem o invasor e ativam os linfócitos B.
Ao serem ativados, os linfócitos B se transformam em plasmócitos, que são células especializadas na produção de grandes quantidades de anticorpos específicos contra a bactéria que foi inicialmente reconhecida pelas células dendríticas.
Esses anticorpos específicos são liberados na corrente sanguínea e se ligam aos antígenos presentes na superfície das bactérias, neutralizando-as. As bactérias imobilizadas pelos anticorpos não só não conseguem mais agir contra as nossas células como também se tornam alvos mais fáceis para a fagocitose por outras células do sistema imune, como macrófagos e neutrófilos.
Exemplo 4: ataque às células tumorais pelas células NK (Natural Killer)
Todos os dias alguma célula do nosso corpo sofre uma mutação indesejável e se torna uma célula neoplásica ou célula tumoral. Se não forem detidas, essas células neoplásicas começaram a se multiplicar rapidamente, formando um tumor.
As células tumorais têm uma característica especial: elas começam a perder os sinais que indicam que são células “normais” do corpo. Esses sinais são proteínas especiais que ficam na superfície da célula e dizem para o sistema imunológico “sou uma célula normal”. Quando essas células perdem essa sinalização, o sistema imunológico entende que há algo errado acontecendo.
As células Natural Killer (NK) agem como “patrulhas de segurança” no nosso corpo, sendo especializadas em encontrar células que não estão normais, como células tumorais (ou células invadidas por vírus). Elas não precisam de muita preparação ou ativação para agir, são rápidas e diretas.
Quando uma célula NK encontra uma célula tumoral, ela rapidamente percebe que aquela célula perdeu os sinais normais de identificação. Ela então se liga à célula tumoral e começa a soltar substâncias tóxicas que têm o objetivo de destruí-la, em um processo semelhante à destruição das células infectadas por vírus. Assim, a célula tumoral é destruída antes que possa se multiplicar e formar um tumor maior.
Por que os leucócitos ficam altos quando temos uma infecção?
Quando o corpo identifica a presença de um agente invasor, como bactérias, vírus, fungos ou parasitas, ele inicia uma resposta coordenada para combater a ameaça. Parte importante dessa resposta envolve o aumento da produção de leucócitos pela medula óssea. Esse aumento na produção de leucócitos visa garantir que haja células de defesa suficientes para combater o patógeno e manter o organismo protegido.
A primeira etapa no aumento da produção de leucócitos começa quando células do sistema imunológico detectam a presença do agente invasor. Essa detecção ocorre por meio de células sentinelas, como macrófagos, células dendríticas e mastócitos, que são células especializadas localizadas nos tecidos que monitoram o ambiente em busca de sinais de patógenos.
Quando essas células reconhecem a presença de patógenos, elas liberam uma série de citocinas e quimiocinas, que são moléculas sinalizadoras que têm a capacidade de induzir inflamação e atrair outras células imunes para o local da infecção. As citocinas também têm uma função importante em sinalizar para a medula óssea que é necessário aumentar a produção de leucócitos para lidar com a ameaça.
A medula óssea, que é o local de produção das células sanguíneas, recebe esses sinais e responde aumentando a atividade das células-tronco hematopoiéticas, induzindo-as a aumentar a produção dos precursores dos leucócitos, que depois se diferenciam nos diversos tipos específicos de leucócitos que o organismo precisa para combater a infecção. Esse processo é conhecido como hematopoiese.
Exemplos de citocinas que estimulam a produção de novos leucócitos são G-CSF, GM-CSF, interleucina-3 (IL-3) e interleucina-6 (IL-6). Cada um deles estimula especificamente a produção e maturação de diferentes leucócitos.
Uma vez que as células-tronco hematopoiéticas recebem os sinais de crescimento, elas começam a se dividir e se diferenciar em células precursoras específicas, cada uma direcionada para se transformar em um tipo específico de leucócito. Esse processo ocorre dentro da medula óssea e, dependendo do tipo de agente invasor e do tipo de citocina liberada, pode aumentar a produção de certos tipos de leucócitos, como:
- Neutrófilos: para lidar com infecções bacterianas.
- Monócitos: que se transformarão em macrófagos para combater infecções crônicas ou para “limpar” áreas danificadas.
- Linfócitos B e T: para respostas imunológicas específicas.
Os leucócitos permanecem na medula óssea até estarem maduros e, em seguida, são liberados na corrente sanguínea para alcançar o local da infecção. Em alguns casos, mesmo leucócitos jovens acabam sendo lançados na circulação, em uma tentativa de neutralizar logo o patógeno.
Durante uma infecção, se colhermos um hemograma diariamente, notaremos inicialmente um aumento no número de leucócitos jovens, especialmente neutrófilos (chamados de bastões) e depois uma elevação dos leucócitos maduros circulando no sangue.
A produção de leucócitos é altamente regulada. À medida que o agente invasor é controlado e eliminado, a necessidade de leucócitos diminui, e os níveis de citocinas estimuladoras também começam a cair. Esse feedback negativo ajuda a impedir uma produção excessiva de leucócitos, evitando possíveis danos aos tecidos saudáveis. As citocinas anti-inflamatórias, como a interleucina-10 (IL-10), ajudam a regular essa produção e a reduzir a resposta inflamatória, garantindo que o sistema imunológico retorne a um estado normal de equilíbrio.
Contagem de leucócitos no sangue
Portanto, como visto até aqui, o número de leucócitos circulando no sangue pode nos trazer informações sobre uma possível infecção em curso. E não só isso, o tipo de leucócito que está aumentado também pode sugerir se o paciente tem uma infecção bacteriana, viral, uma verminose ou mesmo uma reação alérgica.
A quantidade e os tipos de leucócitos circulando no sangue podem ser medidos por meio de um exame laboratorial chamado leucograma. O leucograma faz parte do hemograma, exame que já foi explicado com detalhes no artigo: Hemograma completo (hematócrito, Leucócitos e plaquetas).
O valor normal de leucócitos no sangue varia de 4.000 a 11.000 leucócitos por microlitro (µL). No hemograma, além da contagem total, é feita também a contagem diferencial, que analisa os diferentes tipos de leucócitos presentes no sangue. Essa contagem diferencial pode ser expressa tanto em valores absolutos (número total de cada tipo de célula por microlitro de sangue) quanto em valores percentuais (proporção de cada tipo em relação ao total de leucócitos).
Abaixo, apresentamos os valores normais de referência para cada tipo de leucócito em termos absolutos e percentuais:
Valores de referência dos leucócitos
A tabela abaixo resume os valores considerados normais para os diferentes tipos de leucócitos.
| Tipo de Leucócito | Percentual (%) | Valor normal (células/µL) |
|---|---|---|
| Leucócitos totais | 100% | 4.000 a 11.000 |
| Neutrófilos | 50% a 70% | 2.000 a 7.500 |
| Linfócitos | 20% a 40% | 1.000 a 4.800 |
| Monócitos | 2% a 8% | 100 a 800 |
| Eosinófilos | 1% a 4% | 50 a 400 |
| Basófilos | < 1% | 25 a 100 |
Leucócitos altos (leucocitose)
O aumento no número de leucócitos no sangue, conhecido como leucocitose, ocorre quando há uma contagem total de leucócitos maior do que 11.000 células/µL. A leucocitose pode ser um indicador de várias condições médicas, dependendo de qual tipo específico de leucócito está elevado.
A forma mais comum de leucocitose é por aumento na produção de neutrófilos, quadro chamado de neutrofilia. No entanto, a leucocitose pode surgir em decorrência do aumento de qualquer uma das 5 linhagens de leucócitos no sangue, conforme veremos a seguir.
Neutrofilia (leucocitose por aumento dos neutrófilos)
A neutrofilia é definida como um aumento dos neutrófilos acima dos valores normais (mais de 7.500 células/µL). Ela está comumente associada a infecções e outras condições inflamatórias:
- Infecções bacterianas: a neutrofilia é particularmente comum em infecções bacterianas agudas, pois os neutrófilos são a primeira linha de defesa contra esses patógenos. Exemplos incluem pneumonia bacteriana, faringite, endocardite infecciosa, erisipela e pielonefrite.
- Doenças inflamatórias agudas: inflamações agudas, como em condições como apendicite, colecistite ou pancreatite, também são frequentemente acompanhadas por neutrofilia.
- Estresse físico e emocional: estresse físico, como exercício intenso, trauma ou cirurgia, e até estresse emocional intenso, podem resultar em neutrofilia (geralmente de pequena intensidade).
- Uso de medicamentos: alguns medicamentos, como corticosteroides, podem aumentar a contagem de neutrófilos, pois suprimem a migração dessas células para os tecidos.
- Doenças hematológicas: certas doenças da medula óssea, como leucemia mieloide crônica (LMC), podem causar um aumento significativo no número de neutrófilos.
Linfocitose (leucocitose por aumento dos linfócitos)
A linfocitose é definida como um aumento dos linfócitos acima dos valores normais (mais de 4.800 células/µL em adultos). Ela é frequentemente associada a infecções virais e outras condições crônicas:
- Infecções virais: muitas infecções virais levam à linfocitose, como mononucleose infecciosa, hepatite viral, citomegalovírus ou caxumba.
- Infecções crônicas: algumas bacterianas infecções crônicas, como tuberculose ou sífilis, também podem causar linfocitose.
- Doenças linfoproliferativas: condições como leucemia linfocítica crônica (LLC) ou linfoma resultam em um aumento persistente dos linfócitos no sangue.
- Doenças autoimunes: em alguns casos, como na doença de Addison e em algumas condições autoimunes, também pode haver linfocitose.
Monocitose (leucocitose por aumento dos monócitos)
A monocitose é definida como um aumento dos monócitos acima dos valores normais (mais de 800 células/µL em adultos). Está frequentemente associada a infecções crônicas e outras condições inflamatórias:
- Infecções crônicas: doenças como tuberculose, endocardite bacteriana subaguda, e sífilis frequentemente causam monocitose.
- Doenças autoimunes: algumas doenças autoimunes, como lúpus eritematoso sistêmico (LES) e artrite reumatoide, podem apresentar monocitose, devido à inflamação crônica associada a essas condições.
- Recuperação de infecções agudas: muitas vezes, após uma infecção aguda (bacteriana ou viral), os níveis de monócitos podem aumentar durante a fase de recuperação.
- Doenças hematológicas: leucemias mielomonocíticas e síndrome mielodisplásica são exemplos de doenças hematológicas que podem resultar em monocitose.
Eosinofilia (leucocitose por aumento dos eosinófilos)
A eosinofilia é definida como um aumento dos eosinófilos acima dos valores normais (mais de 400 células/µL em adultos). Está frequentemente associada a condições alérgicas e infecções parasitárias:
- Infecções parasitárias: infecções por vermes, como esquistossomose, ascaridíase ou outras infecções parasitárias, frequentemente resultam em eosinofilia, dado que os eosinófilos são especializados no combate a parasitas multicelulares.
- Alergias e asma: condições alérgicas, como asma, rinite alérgica e dermatite atópica, podem causar eosinofilia. Os eosinófilos desempenham um papel importante na resposta imune associada a alergias.
- Doenças autoimunes e inflamatórias: algumas condições autoimunes e inflamatórias, como a doença de Crohn e a vasculite eosinofílica, podem levar a um aumento dos eosinófilos.
- Síndrome hipereosinofílica: condição rara na qual há uma proliferação excessiva e persistente de eosinófilos, levando a danos aos tecidos.
Basofilia (leucocitose por aumento dos basófilos)
A basofilia é definida como um aumento dos basófilos acima dos valores normais (mais de 100 células/µL em adultos). É uma condição menos comum e pode estar associada a várias condições inflamatórias e hematológicas:
- Alergias e reações alérgicas: reações alérgicas graves, como anafilaxia, podem causar basofilia. Os basófilos liberam histamina, que desempenha um papel importante nas reações alérgicas.
- Doenças hematológicas: leucemia mieloide crônica (LMC) e outras neoplasias mieloproliferativas são causas comuns de basofilia. Nessas condições, ocorre uma produção excessiva de células sanguíneas, incluindo basófilos.
- Doenças inflamatórias crônicas: algumas doenças inflamatórias crônicas, como artrite reumatoide e colite ulcerativa, podem estar associadas à basofilia.
Falamos mais sobre a leucocitose e suas causas no artigo: Leucocitose (leucócitos altos): o que é, causas e tratamento.
Leucócitos baixos (leucopenia)
Leucopenia é a condição na qual ocorre uma diminuição do número total de leucócitos no sangue, geralmente abaixo de 4.000 células/µL.
A leucopenia pode ser causada por uma série de condições médicas e fatores que afetam a produção ou sobrevivência dos leucócitos.
Principais causas de leucopenia
- Infecções virais: muitas infecções virais, como hepatite, HIV ou dengue, podem causar uma redução temporária dos leucócitos.
- Medicamentos: alguns medicamentos, como quimioterápicos usados no tratamento do câncer, imunossupressores e certos antibióticos, podem afetar a produção de leucócitos pela medula óssea.
- Doenças da medula óssea: condições que comprometem a medula óssea, como leucemia, síndromes mielodisplásicas ou anemia aplástica, podem levar à leucopenia por reduzirem a capacidade de produção de leucócitos.
- Doenças autoimunes: doenças como lúpus eritematoso sistêmico podem atacar a medula óssea ou os próprios leucócitos, resultando em uma redução da contagem.
- Deficiências nutricionais: a falta de nutrientes essenciais, como vitamina B12, folato e cobre, pode prejudicar a produção normal de leucócitos.
- Radioterapia e exposição à radiação: exposição à radiação ionizante, seja em tratamentos oncológicos ou por motivos ambientais, pode prejudicar a função da medula óssea e causar leucopenia.
A leucopenia em si não causa sintomas específicos, mas as suas consequências são perceptíveis devido ao enfraquecimento do sistema imunológico. Pacientes com leucopenia apresentam maior risco de desenvolver infecções frequentes e severas, especialmente infecções oportunistas.
Como surge a leucemia?
A leucemia surge quando uma mutação genética ocorre em uma dessas células-tronco hematopoiéticas ou em suas células precursoras. Essas mutações podem ser adquiridas ao longo da vida (não hereditárias) e ocorrem em resposta a vários fatores de risco ou de forma espontânea. Essas alterações genéticas causam uma mudança no comportamento das células da medula óssea, que passam a se dividir de maneira descontrolada, sem obedecer aos sinais normais de crescimento e morte celular.
Na leucemia, as células mutadas da medula óssea perdem a capacidade de se diferenciar corretamente em células maduras. Em vez disso, elas permanecem em um estado imaturo e continuam a se dividir. Essas células imaturas são chamadas de blastos, que não conseguem desempenhar a função de células sanguíneas maduras e começam a se acumular tanto na medula óssea quanto no sangue periférico. A presença excessiva de blastos é uma característica marcante da leucemia.
A acumulação de blastos na medula óssea impede a produção normal de células sanguíneas saudáveis. Isso causa uma redução de hemácias (anemia), plaquetas (trombocitopenia) e leucócitos funcionais (leucopenia ou imunodeficiência). A anemia, a baixa contagem de plaquetas e o comprometimento da imunidade são os principais responsáveis pelos sintomas apresentados por pessoas com leucemia.
Os valores dos leucócitos no sangue em pacientes com leucemia podem variar bastante dependendo do tipo de leucemia (aguda ou crônica) e de outros fatores específicos da doença e do paciente. Em geral, o valor dos leucócitos em casos de leucemia pode estar significativamente alterado, apresentando-se muito elevado ou, em alguns casos, até mesmo reduzido, refletindo as diferentes manifestações dessa doença.
A tabela abaixo resume os valores dos leucócitos no sangue em pacientes com leucemia
| Tipo de Leucemia | Valor Típico de Leucócitos (células/µL) |
| Leucemia Mieloide Crônica (LMC) | Geralmente entre 100.000 a 500.000, podendo ser muito alto. |
| Leucemia Linfocítica Crônica (LLC) | Normalmente entre 20.000 a 200.000. |
| Leucemia Mieloide Aguda (LMA) | Pode variar bastante, de 15.000 a mais de 100.000, com grande presença de blastos. |
| Leucemia Linfocítica Aguda (LLA) | Varia de valores normais a elevados, frequentemente 20.000 a 100.000, com presença de blastos. |
Falamos especificamente da leucemia no artigo: Leucemia: tipos, sintomas e tratamento.
Leucócitos na urina
Além do exame de sangue, podemos também encontrar leucócitos no exame simples de urina, conhecido como EAS ou urina tipo 1.
A presença de leucócitos na urina, conhecida como leucocitúria, é um sinal de que há uma inflamação ou infecção em algum ponto do trato urinário.
Em geral, a quantidade de leucócitos na urina é mínima. Se o paciente desenvolve leucocitúria, é porque algo no sistema urinário está ativando o sistema imunológico e recrutando leucócitos para o trato urinário.
Os leucócitos migram dos vasos sanguíneos através do tecido afetado para chegar ao local da infecção ou inflamação. Portanto, qualquer processo inflamatório ou infeccioso na bexiga, uretra, ureter ou rins provocará a presença de leucócitos na urina.
Principais causas de leucócitos na urina
A leucocitúria é um achado comum em exames de urina (EAS) e pode ter várias causas, incluindo:
1. Infecção do Trato Urinário (ITU)
Uma infecção do trato urinário é uma das causas mais comuns de leucócitos na urina. Pode ocorrer em diferentes partes do trato urinário, como:
- Cistite: infecção da bexiga, frequentemente causada por bactérias como Escherichia coli. A resposta imune a essa bactéria resulta em inflamação da bexiga e migração de leucócitos, que são excretados na urina (leia: Cistite: o que é, sintomas e tratamento).
- Pielonefrite: infecção dos rins, que geralmente ocorre devido à ascensão de uma infecção da bexiga. A resposta inflamatória nos rins leva ao acúmulo de leucócitos na urina (leia: Pielonefrite (infecção renal)).
- Uretrite: inflamação da uretra. Pode ser devido a uma infecção bacteriana ou até por doenças sexualmente transmissíveis, como clamídia ou gonorreia (leia: Uretrite: o que é, causas, sintomas e tratamento).
2. Inflamações do trato urinário sem infecção bacteriana
Leucócitos na urina podem ser encontrados também em situações de inflamação que não envolvem infecções bacterianas, tais como:
- Cistite Intersticial: uma inflamação crônica da bexiga que não está associada a uma infecção bacteriana pode resultar na presença de leucócitos na urina (leia: Cistite Intersticial: síndrome da bexiga dolorosa).
- Glomerulonefrite: inflamações dos glomérulos renais podem causar a presença de leucócitos e outras células na urina (leia: Glomerulonefrite: o que é, sintomas e tratamento).
- Cálculos renais: os cálculos podem arranhar as paredes do trato urinário e criar áreas de inflamação local, atraindo leucócitos como parte do processo inflamatório (leia: Cálculo renal (pedra no rim): causas, tipos e tratamento).
- Nefrite intersticial: inflamação do tecido renal, geralmente de origem alérgica. Costuma causar aumento do número de eosinófilos na urina.
Referências
- Brunwald, E., Hauser, S.L., Fauci, A.S., Longo, D.L., Kasper, D.L., Jameson, J.L. (Eds.). Harrison’s Principles of Internal Medicine. 20ª edição. Nova York: McGraw-Hill Education, 2018.
- Hall, J.E. Guyton & Hall: Tratado de Fisiologia Médica. 14ª edição. Elsevier, 2020.
- Kaushansky, K., Lichtman, M.A., Prchal, J.T., Levi, M., Press, O.W., Burns, L.J., Caligiuri, M. Williams Hematology. 10ª edição. Nova York: McGraw-Hill Education, 2021.
- Histology, White Blood Cell – StatPearls.
- The role of neutrophils in host defense and disease – The Journal of allergy and clinical immunology.
- Approach to the patient with neutrophilia – UpToDate.
- Hyperleukocytosis and leukostasis in hematologic malignancies – UpToDate.
- Evaluation of Patients with Leukocytosis – American Family Physician.
- Leukocytosis – StatPearls.
Autor(es)
Médico graduado pela Universidade Federal do Rio de Janeiro (UFRJ), com títulos de especialista em Medicina Interna e Nefrologia pela Universidade Estadual do Rio de Janeiro (UERJ), Sociedade Brasileira de Nefrologia (SBN), Universidade do Porto e pelo Colégio de Especialidade de Nefrologia de Portugal.





Leave a Comment